Betabloqueadores en Urgencias Toxicológicas
María Luisa Cárdenas M.
Médica Magíster en Farmacología
Profesora Asociada Universidad Nacional de Colombia
Médica Magíster en Farmacología
Profesora Asociada Universidad Nacional de Colombia
Generalidades de los Betabloqueadores:
Son fármacos antagonistas de los receptores beta adrenérgicos, que se utilizan ampliamente para el manejo de la hipertensión arterial, angina de pecho, para arritmias como el caso del Propranolol, para la profilaxis de la migraña o tópicamente para el manejo del glaucoma como el caso del Timolol.
De acuerdo a su afinidad sobre los receptores beta adrenérgicos se pueden clasificar en:
• Betabloqueadores cardioselectivos ß1.
• Betabloqueadores No cardioselectivos ß1, ß2.
• Betabloqueadores No cardioselectivos ß1, ß2.
En general, los betabloqueadores tienen una biotransformación hepática y de los no cardioselectivos se debe resaltar la cinética del propranolol pues sufre metabolismo de primer paso, lo cual incide en su baja biodisponibilidad. Uno de los aspectos más importantes de los betabloqueadores radica en su liposolubilidad, pues de ella depende el que se presenten reacciones adversas específicamente sobre el Sistema Nervioso Central. La concentración máxima se alcanza entre 1 – 4 horas pero puede mantenerse una concentración estable si se utilizan las formas farmacéuticas de liberación sostenida o retardada; la eliminación en su mayoría se hace después de ser metabolizados en hígado y sólo un porcentaje pequeño se elimina por vía renal sin cambios.
Mecanismo de Acción de los Betabloqueadores:
Los antagonistas beta adrenérgicos se caracterizan por tener afinidad por los receptores beta pero carecen de actividad intrínseca, es decir, no son capaces de generar una señalización transmembrana que facilite la producción de una respuesta celular. Sin embargo, algunos de ellos como el pindolol y el metoprolol tienen la propiedad de ser agonistas parciales, es decir, de poseer una leve actividad intrínseca denominada Actividad Simpaticomimética Intrínseca (ASI), que le permite ser utilizados en situaciones especiales donde los efectos adversos son intolerables para el paciente o agravan una condición patológica concomitante.
Tabla No. 34. Parámetros farmacocinéticos y farmacodinámicos de los betabloqueadores
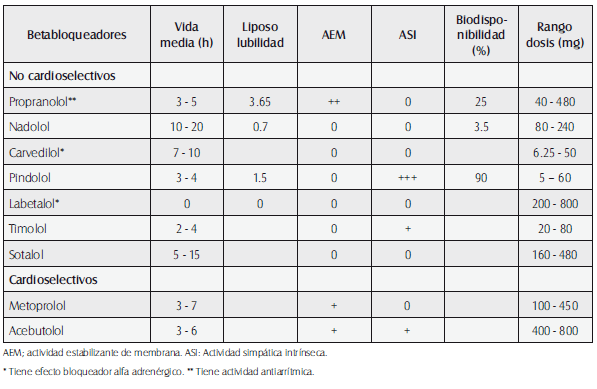
Dosis Tóxica:
La respuesta que manifiestan los pacientes a la sobredosis es variable de acuerdo a la patología de base, las características farmacocinéticas y al agente bloqueador que se haya ingerido, pudiéndose presentar reacciones fatales.
Aunque no se tienen definidos unos límites claros, se podría decir que el ingerir 2 – 3 veces la dosis terapéutica, se puede considerar como un alto riesgo de toxicidad. El betabloqueador que se considera de menor riesgo es el pindolol por tener una mayor actividad simpaticomimética intrínseca.
Manifestaciones Clínicas:
1. ALTERACIONES CARDIOVASCULARES: por su propio mecanismo de acción, la bradicardia y la hipotensión son las primeras manifestaciones y las más comunes. El bloqueo aurículo ventricular y el shock cardiogénico se presentan con sobredosis muy altas, en especial, con betabloqueadores como el propranolol. En el electrocardiograma se puede evidenciar un incremento del intervalo PR y la ausencia del complejo QRS que ocurre con altas sobredosis.
2. ALTERACIONES SOBRE SISTEMA NERVIOSO CENTRAL: los betabloqueadores con mayor liposolubilidad y con propiedad estabilizadora de membrana como el propranolol son los que podrían ocasionar manifestaciones como las convulsiones, coma y paro respiratorio.
3. ALTERACIONES SOBRE SISTEMA RESPIRATORIO: el broncoespasmo puede presentarse cuando se han utilizado betabloqueadores no cardioselectivos en pacientes con antecedentes de Enfermedad Pulmonar Obstructiva Crónica (EPOC) o asma bronquial, en los cuales se incrementa el tono del músculo liso bronquial al realizar el bloqueo de los receptores beta 2 bronquiales.
4. OTRAS ALTERACIONES: se puede presentar hipoglicemia, especialmente en pacientes que estén recibiendo terapia antidiabética, en los que se dificulta evidenciar una respuesta hipoglicémica por tener el bloqueo betaadrenérgico.
Laboratorio:
Se deben realizar análisis paraclínicos como electrolitos, glucemia, BUN, creatinina, gases arteriales y electrocardiograma.
Tratamiento:
Se recomienda seguir el manejo propuesto en el capítulo Manejo del paciente intoxicado en el servicio de urgencias.
Las consideraciones especiales que se deben tener en cuenta en este tipo de intoxicación son:
1. MEDIDAS DE SOPORTE Y EMERGENCIA
a. Mantener vía aérea permeable
b. Manejo sintomático para las convulsiones, hipotensión o hipoglicemia
c. Manejo del broncoespasmo con broncodilatadores si este se presenta.
b. Manejo sintomático para las convulsiones, hipotensión o hipoglicemia
c. Manejo del broncoespasmo con broncodilatadores si este se presenta.
2. MEDIDAS PARA DISMINUIR ABSORCIÓN
a. Lavado gástrico si son altas las dosis ingeridas
b. Administrar carbón activado
c. La hemodiálisis o la hemoperfusión puede ser útil, especialmente, para aquellos betabloqueadores que no son altamente liposolubles como el sotalol.
b. Administrar carbón activado
c. La hemodiálisis o la hemoperfusión puede ser útil, especialmente, para aquellos betabloqueadores que no son altamente liposolubles como el sotalol.
3. FÁRMACOS ESPECÍFICOS
a. Glucagon 3 – 10 mg/kg IV en bolo, seguidos por una infusión de 1 – 5 mg/h en infusión continua. Niños: 0.15 mg/kg en bolo seguido de 0.05 – 0.1 mg/kg/h. (Diluir 4 mg en 50 ml de DAD 5% para infusión continua).
b. Epinefrina infusión de 1 – 4 mcg/min de acuerdo con la respuesta.
c. Bicarbonato de sodio para intoxicaciones por propranolol en dosis de 1- 2 mEq/kg
d. Isoproterenol en infusión: En caso de la Torsan de Pointes por ingestión de sotalol en dosisde 0.5 – 1 mcg/min IV. Niños: 0.1 mcg/kg/ min. Las preparaciones se pueden degradar o tornarse oscuras por exposición a luz, aire o calor.
b. Epinefrina infusión de 1 – 4 mcg/min de acuerdo con la respuesta.
c. Bicarbonato de sodio para intoxicaciones por propranolol en dosis de 1- 2 mEq/kg
d. Isoproterenol en infusión: En caso de la Torsan de Pointes por ingestión de sotalol en dosisde 0.5 – 1 mcg/min IV. Niños: 0.1 mcg/kg/ min. Las preparaciones se pueden degradar o tornarse oscuras por exposición a luz, aire o calor.
Lecturas recomendadas:
1. Love, J.N. et al. ”Electrocardiographic changes associated with beta-blocker toxicity”. Ann Emerg Med 2002; 40: 603 – 610
2. Oses, I. et al. ”Intoxicaciones mediamentosas psicofármacos y antiarrítmicos”. Anales Sis San Navarra 2003; 26 (Supl I): 49 – 63
3. Goodman, G. y Gilman, G. Bases Farmacológicas de la Terapeútica. 10ª Edición. McGraw- Hill, 2005
4. Opie, G. Fármacos en cardiología. México: McGraw-Hill. 2002.
5. Olson, K. R. Poisoning & Drug Overdose. USA: 5a Edition, McGraw-Hill, 2007.
2. Oses, I. et al. ”Intoxicaciones mediamentosas psicofármacos y antiarrítmicos”. Anales Sis San Navarra 2003; 26 (Supl I): 49 – 63
3. Goodman, G. y Gilman, G. Bases Farmacológicas de la Terapeútica. 10ª Edición. McGraw- Hill, 2005
4. Opie, G. Fármacos en cardiología. México: McGraw-Hill. 2002.
5. Olson, K. R. Poisoning & Drug Overdose. USA: 5a Edition, McGraw-Hill, 2007.
