Enfermedades Infecciosas y Microbiología Clínica
Vol. 28. Núm. 9.
páginas 577-668 (Noviembre 2010https://www.elsevier.es/es-revista-enfermedades-infecciosas-microbiologia-clinica-28-articulo-hipopotasemia-con-funcion-renal-normal-S0213005X10000777?referer=buscador
Sr. Director:
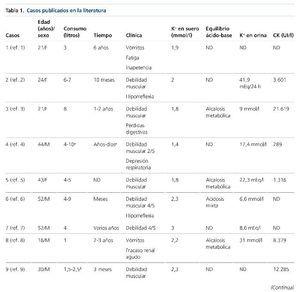
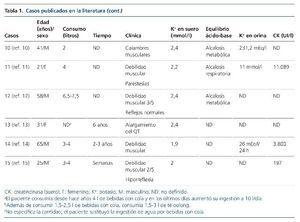
El tenofovir es un análogo de nucleótido inhibidor de la transcriptasa inversa aprobado en el año 2001 para el tratamiento de la infección por el virus de la inmunodeficiencia humana. Actualmente es uno de los agentes antirretrovirales más prescritos en Europa y Estados Unidos. Es un fármaco muy bien tolerado. Los efectos secundarios más comunes son náuseas, vómitos y pérdida de apetito, aunque también se han descrito alteraciones hepáticas y renales, como insuficiencia renal, necrosis tubular aguda, tubulopatía proximal tipo Fanconi, proteinuria y diabetes insípida1. Recientemente, en nuestro país se ha publicado un caso de hipopotasemia grave no asociada a insuficiencia renal2 en relación con la administración de tenofovir. Asimismo, se han descrito casos en los que existen otros factores concomitantes favorecedores de toxicidad renal además de tenofovir3. La estrategia de búsqueda bibliográfica se ha basado en la introducción de las palabras clave mencionadas en la base de datos PubMed.
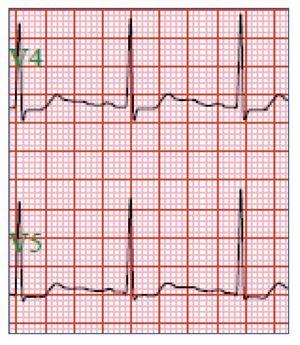
Se presenta el caso clínico de una mujer de 42 años diagnosticada en 1990 de infección por el virus de la inmunodeficiencia humana en tratamiento con tenofovir/emtricitabina (245/200mg/día), lopinavir/ritonavir (400/100mg/12h) y saquinavir (1.000mg/12h) desde hacía 2 años y medio. El número de los linfocitos T CD4+ era de 427 elementos/ml y la carga viral era de 4.500 copias de ARN/ml. No recibía otros fármacos. Ingresó por impotencia funcional de predominio en las extremidades inferiores y debilidad generalizada de varios días de evolución. La exploración física no mostraba hallazgos de interés, a excepción de un equilibrio muscular de 4+/5 en ambos cuádriceps y abolición de los reflejos musculares profundos rotulianos y aquíleos. En la analítica de sangre se observó potasio de 2,32mmol/l, sodio, fósforo, calcio y magnesio dentro de los límites normales, creatinina de 1mg/dl, aspartato aminotransferasa de 243UI/l, alanina aminotransferasa de 252UI/l y albúmina de 4,23g/dl. Un electrocardiograma no mostró alteraciones significativas. Una radiografía de tórax y abdomen y una ecografía abdominal no evidenciaron alteraciones destacables. Para el estudio de la clínica neurológica se realizó una punción lumbar, en la que solo destacó proteinorraquia de 64mg/dl. Una tomografía computarizada puso de manifiesto una atrofia cerebral de predominio cortical. En un electromiograma de las extremidades inferiores se observó la existencia de una polineuropatía sensitiva distal y una polirradiculopatía axonal de predominio proximal L4-S1. Una resonancia magnética lumbar informó de un colapso del saco dural a nivel lumbar que fue indicativo de cirugía descompresiva. El estudio de la hipopotasemia incluyó un equilibrio acidobásico (pH de 7,48, pCO2 de 53,0mmHg, pO2 de 54,9mmHg, bicarbonato de 36,8mmol/l y exceso de base de 13,2mmol/l), un aclaramiento de creatinina de 74,5ml/min, un sodio de 77mEq/l y un potasio de 54mEq/l en orina. Los niveles de aldosterona fueron de 5ng/dl (dentro de rango normal, según nuestro laboratorio). La alcalosis metabólica y la hipopotasemia se corrigieron en primera instancia mediante la administración de cloruro potásico, si bien tras su retirada reapareció la hipopotasemia (2,52mmol/l). Esta situación revirtió de forma definitiva con la supresión del tratamiento antirretroviral con tenofovir y su sustitución por raltegravir, ritonavir y darunavir y una nueva reposición con cloruro potásico en un tiempo global aproximado de 15 días.
La disfunción tubular renal proximal, normalmente asociada a disminución de la tasa de filtración glomerular, es una complicación conocida y generalmente reversible del tratamiento con tenofovir. Los signos de esta disfunción pueden incluir hipopotasemia, hipofosfatemia, proteinuria, glucosuria normoglucémica, acidosis tubular renal proximal tipo ii y diabetes insípida4. Se postula que ciertas variaciones en los genes que codifican para las proteínas transportadoras de la membrana podrían condicionar una acumulación intracelular de tenofovir que favorecería la toxicidad mitocondrial causante de defectos ultraestructurales del túbulo renal proximal5,6. No obstante, en nuestro caso, la función renal era normal y la presencia de hipopotasemia asociada a alcalosis metabólica en vez de a la acidosis metabólica hiperclorémica característica de la acidosis tubular renal proximal tipo ii podría señalar la presencia de toxicidad renal a la altura del asa de Henle o el túbulo contorneado distal en similitud al síndrome de Bartter/Gitelman. La reaparición de la alcalosis hipopotasémica tras la retirada de la reposición iría a favor del origen tubular de ésta.
Los factores relacionados con la nefrotoxicidad por tenofovir son la presencia de enfermedad renal crónica previa, el uso simultáneo de fármacos nefrotóxicos, un peso corporal bajo, la edad avanzada y un recuento bajo de los linfocitos CD47,8. En algunos estudios clínicos se ha descrito un aumento en la incidencia de efectos adversos renales al administrar tenofovir con ciertos fármacos antirretrovirales, como didanosina9,10 o inhibidores de la proteasa potenciados con ritonavir2 (como sucedía en nuestro caso y el previamente publicado). Con el objetivo de reducir el riesgo de toxicidad renal asociada a tenofovir se recomienda el cálculo del filtrado glomerular renal o una estimación del aclaramiento de creatinina en la evaluación médica inicial. La monitorización periódica de la función renal debería realizarse como parte del control habitual y con mayor frecuencia si la función renal fluctúa4. Habría que suspender su uso si la función renal disminuye progresivamente y no se identifica otra causa de fracaso renal o existen signos de disfunción tubular renal proximal o, al igual que en nuestro caso, hipopotasemia, una vez que se descarten otras causas, como pérdidas digestivas o cutáneas o la presencia de hiperaldosteronismo.
Como conclusión hay que pensar en el tenofovir como causa de hipopotasemia aún en presencia de una función renal normal. Debería hacerse un seguimiento estrecho de la función renal y los electrólitos en pacientes tratados con este fármaco, especialmente ante la presencia conjunta de factores favorecedores de toxicidad renal. Tanto la hipopotasemia como la mayoría de las alteraciones renales asociadas a tenofovir suelen ser reversibles tras la retirada de este.