Transfusiones de sangre después de un trauma
Una propuesta de estratificación del riesgo para guiar la necesidad de transfusiones en el trauma.Autor: Druin Burch Fuente: Plos Medicine Blood Transfusions following Trauma: Finding an Evidence-Based Vein
Las muertes por lesiones representan seis millones de muertes al año, un tercio más que la malaria, la tuberculosis y el VIH combinados. [1] En PLoS Medicine, Pablo Perel y sus colegas reportaron que la hemorragia mata al 30% a 40% de los que mueren a causa de las lesiones. Su artículo de investigación sugiere que una fracción importante de las muertes relacionadas con el trauma podría evitarse a través de simplemente mejorar nuestro conocimiento de cuándo administras transfusiones de sangre a los pacientes que sufren un trauma [2]. "A pesar de que a menudo se utilizan glóbulos rojos (GR) alogénicos en el tratamiento de pacientes con traumatismo hemorrágico", escriben, "existe una considerable incertidumbre sobre el balance entre sus riesgos y beneficios."
La transfusión de sangre es una intervención costosa que no siempre mejora los resultados clínicos (averiguarlo puede ser difícil o imposible para un observador saberlo) y sobre la que se han reconocido peligros, incluyendo los inmunológicos y los riesgos infecciosos.
A pesar de estar en uso durante mucho tiempo -el primer aumento de las transfusiones de sangre por lesiones fue impulsado por la Primera Guerra Mundial que comenzó hace un siglo- sabemos muy poco sobre cuándo es mejor usarlas. De hecho, puede ser que con la transfusión, al igual que con tantas otras cosas, la frase los "riesgos y beneficios" refuerza el hábito médico optimista pero engañoso, de asumir la existencia de beneficios y de no cuantificar el riesgo de los daños.
El artículo de investigación de Perel y colegas presenta un análisis de los datos recogidos en el marco del estudio CRASH-2 de ácido tranexámico en el traumatismo [3]. El CRASH-2 evalúa una intervención existente para la que ninguna empresa posee patente: la reducción de la mortalidad demostrada por el estudio es un buen ejemplo de los beneficios que se pueden obtener a partir de las probar correctamente terapias que han existido por mucho tiempo, pero nunca se han evaluado suficientemente. La transfusión de glóbulos rojos es un próximo objetivo obvio.
Es difícil justificar que la ciencia médica supervise la transfusión de 80 millones de unidades de sangre cada año, a un costo por unidad desde 40 dólares [4] a $ 1183 dólares [5], al mismo tiempo que no saber si lo que hace puede conferir daños graves o importantes beneficios y sin tener todavía investigado de manera fiable cómo disminuir los primeros y maximizar los segundos.
Los estudios observacionales han indicado que la transfusión de sangre en el trauma se asocia con malos resultados, pero el potencial para la confusión es tan obvio como la correlación entre la hemorragia grave y las lesiones graves.
Aquellos que tienen mayor riesgo de morir experimentan un odds ratio (OR) de 0,59 (95% intervalo de confianza [IC] desde 0,47 hasta 0,74) de muerte si se transfunden, mientras que aquellos en el grupo de riesgo del 21% -50% no ven ninguna diferencia significativa en su OR para morir en función de si se transfunden o no (OR 0.92, IC del 95%: 0,78 a 1,08).
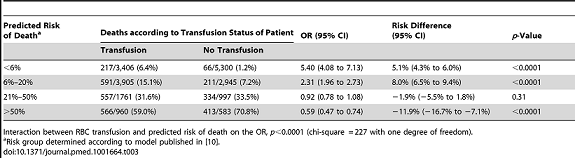
Mortalidad según estratificación predictiva del riesgo(cateogrías)
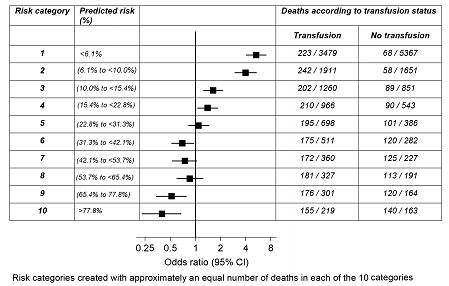
Odds ratio para muerte comparando transfusión vs no transfusión según riesgo
Nuestra incertidumbre acerca de la cantidad de sangre a administrar y cuándo proporcionarla, no sólo en el trauma, sino también en otros ámbitos, se conoce desde hace largo tiempo, y los ensayos recientes de hemorragia gastrointestinal [7] cirugía ortopédica [8], y en el infarto agudo de miocardio [9 ] han tendido a mostrar que cuando se comparan una estrategia de transfusión liberal con una conservadora a través de una serie de criterios de valoración, la estrategia conservadora es mejor.
Usar los datos de la observación -incluso ajustados por factores de confusión conocidos- tiene limitaciones. En ese sentido, el estudio realizado por Perel y sus colegas simplemente nos recuerda que la cantidad de sangre a dar, y cuándo, es todavía un área importante de incertidumbre.
La verdadera originalidad del estudio se encuentra en su demostración de que el riesgo asociado a la transfusión se desplaza de manera considerable cuando los pacientes de trauma se estratifican por la gravedad de su presentación.
Otro trabajo reciente [10] ha puesto de manifiesto que el riesgo de infección por transfusión de sangre no puede limitarse a los virus transmitidos por la sangre, lo que demuestra que las estrategias de transfusión restrictivas están asociadas con un número reducido de infecciones relacionadas con la atención de la salud.
Estas exploraciones acerca de por qué una transfusión puede causar daño son interesantes, pero no se ocupan de lo que más necesitamos saber: explicar el daño no es tan importante como evitarlo.
El papel de la hemoglobina y la medición del hematocrito en el manejo inicial del trauma merece consideración, y era Perel y colaboradores carecían de los datos para tratarlo. Como resultado, existe la posibilidad de que las mediciones iniciales más bajas de hemoglobina o del hematocrito que se pueden inferir sobre la base de los estratos de riesgo podrían ser un factor de confusión que vincula la probabilidad de transfusión de sangre con la muerte.
Sin embargo, poco después de un traumatismo (en el estudio CRASH-2 los pacientes fueron incluidos dentro de las ocho horas de la lesión, siendo la media de menos de tres horas [3]), la determinación de hemoglobina y del hematocrito son confiables. Basar las estrategias de transfusión en las variables fisiológicases probable que sea, como argumentan los autores, más útil que basarlas en mediciones de laboratorio iniciales.
Las transfusiones de glóbulos rojos pueden costar vidas también, y es posible, y quizá probable, que lo hagan en algunos casos dentro de los umbrales de hemoglobina y clínicos actualmente en uso. El trauma y las transfusiones son demasiado comunes y demasiado costosos como para que toleremos esta incertidumbre.
Aunque Perel y sus colegas describen su artículo como "informativo para la práctica clínica actual", su valor radica en que nos dice que la práctica clínica actual está peligrosamente desinformada. Lo hace de una manera tal que sugiere persuasivamente que los ensayos futuros acerca de la transfusión en el trauma deben tener en cuenta la gravedad de la presentación de un paciente.
Nuestra base de pruebas para transfusiones en trauma es aún pobre. Con tantos pacientes que mueren cada año, y con las muertes por lesiones que aumentará en importancia a medida que los accidentes de tránsito y las lesiones violentas representan una mayor parte de la carga mundial de la enfermedad [12], tenemos una razón de peso para mejorar y racionalizar nuestras estrategias de transfusión de sangre.
La transfusión de sangre es una intervención costosa que no siempre mejora los resultados clínicos (averiguarlo puede ser difícil o imposible para un observador saberlo) y sobre la que se han reconocido peligros, incluyendo los inmunológicos y los riesgos infecciosos.
A pesar de estar en uso durante mucho tiempo -el primer aumento de las transfusiones de sangre por lesiones fue impulsado por la Primera Guerra Mundial que comenzó hace un siglo- sabemos muy poco sobre cuándo es mejor usarlas. De hecho, puede ser que con la transfusión, al igual que con tantas otras cosas, la frase los "riesgos y beneficios" refuerza el hábito médico optimista pero engañoso, de asumir la existencia de beneficios y de no cuantificar el riesgo de los daños.
El artículo de investigación de Perel y colegas presenta un análisis de los datos recogidos en el marco del estudio CRASH-2 de ácido tranexámico en el traumatismo [3]. El CRASH-2 evalúa una intervención existente para la que ninguna empresa posee patente: la reducción de la mortalidad demostrada por el estudio es un buen ejemplo de los beneficios que se pueden obtener a partir de las probar correctamente terapias que han existido por mucho tiempo, pero nunca se han evaluado suficientemente. La transfusión de glóbulos rojos es un próximo objetivo obvio.
Es difícil justificar que la ciencia médica supervise la transfusión de 80 millones de unidades de sangre cada año, a un costo por unidad desde 40 dólares [4] a $ 1183 dólares [5], al mismo tiempo que no saber si lo que hace puede conferir daños graves o importantes beneficios y sin tener todavía investigado de manera fiable cómo disminuir los primeros y maximizar los segundos.
Los estudios observacionales han indicado que la transfusión de sangre en el trauma se asocia con malos resultados, pero el potencial para la confusión es tan obvio como la correlación entre la hemorragia grave y las lesiones graves.
"Una mayor probabilidad inicial de la muerte se asocia con un mayor beneficio de la transfusión de glóbulos rojos"
Mediante el uso de un modelo validado [6] para categorizar a los pacientes en cuatro estratos predefinidos de riesgo de morir (<6%, 6% -20%, 21% -50%, y mayor que 50% de probabilidad de muerte) sobre la base de observaciones clínicas iniciales, el presente estudio demuestra que: una mayor probabilidad inicial de la muerte se asocia con un mayor beneficio de la transfusión de glóbulos rojos.Aquellos que tienen mayor riesgo de morir experimentan un odds ratio (OR) de 0,59 (95% intervalo de confianza [IC] desde 0,47 hasta 0,74) de muerte si se transfunden, mientras que aquellos en el grupo de riesgo del 21% -50% no ven ninguna diferencia significativa en su OR para morir en función de si se transfunden o no (OR 0.92, IC del 95%: 0,78 a 1,08).

Mortalidad según estratificación predictiva del riesgo(cateogrías)

Odds ratio para muerte comparando transfusión vs no transfusión según riesgo
"Dentro de los estratos de menor riesgo, la transfusión no se asocia con un beneficio pero sí con daño"
Para aquellos dentro de los estratos de menor riesgo, la transfusión no se asocia con un beneficio pero sí con daño. Los pacientes con un 6% a un 20% de probabilidad de muerte tenían un OR de 2,31 (IC del 95%: 1,96 a 2,73) para morir si recibían una transfusión, mientras que para aquellos cuyo riesgo inicial era por debajo del 6%, el OR para la mortalidad asociada con la transfusión era 5,40 (IC del 95% 4.8 a 7.13). Estos hallazgos son convincentes.Nuestra incertidumbre acerca de la cantidad de sangre a administrar y cuándo proporcionarla, no sólo en el trauma, sino también en otros ámbitos, se conoce desde hace largo tiempo, y los ensayos recientes de hemorragia gastrointestinal [7] cirugía ortopédica [8], y en el infarto agudo de miocardio [9 ] han tendido a mostrar que cuando se comparan una estrategia de transfusión liberal con una conservadora a través de una serie de criterios de valoración, la estrategia conservadora es mejor.
Usar los datos de la observación -incluso ajustados por factores de confusión conocidos- tiene limitaciones. En ese sentido, el estudio realizado por Perel y sus colegas simplemente nos recuerda que la cantidad de sangre a dar, y cuándo, es todavía un área importante de incertidumbre.
La verdadera originalidad del estudio se encuentra en su demostración de que el riesgo asociado a la transfusión se desplaza de manera considerable cuando los pacientes de trauma se estratifican por la gravedad de su presentación.
"Explicar el daño no es tan importante como evitarlo"
Un posible mecanismo por el que la transfusión puede matar es a través de los eventos oclusivos vasculares. Perel y sus colegas señalan que para los que están en el riesgo más bajo de muerte predicho, estos acontecimientos tuvieron un OR de 4,92 (IC del 95%: 2,80 a 8,65) asociado a la transfusión de glóbulos rojos.Otro trabajo reciente [10] ha puesto de manifiesto que el riesgo de infección por transfusión de sangre no puede limitarse a los virus transmitidos por la sangre, lo que demuestra que las estrategias de transfusión restrictivas están asociadas con un número reducido de infecciones relacionadas con la atención de la salud.
Estas exploraciones acerca de por qué una transfusión puede causar daño son interesantes, pero no se ocupan de lo que más necesitamos saber: explicar el daño no es tan importante como evitarlo.
El papel de la hemoglobina y la medición del hematocrito en el manejo inicial del trauma merece consideración, y era Perel y colaboradores carecían de los datos para tratarlo. Como resultado, existe la posibilidad de que las mediciones iniciales más bajas de hemoglobina o del hematocrito que se pueden inferir sobre la base de los estratos de riesgo podrían ser un factor de confusión que vincula la probabilidad de transfusión de sangre con la muerte.
Sin embargo, poco después de un traumatismo (en el estudio CRASH-2 los pacientes fueron incluidos dentro de las ocho horas de la lesión, siendo la media de menos de tres horas [3]), la determinación de hemoglobina y del hematocrito son confiables. Basar las estrategias de transfusión en las variables fisiológicases probable que sea, como argumentan los autores, más útil que basarlas en mediciones de laboratorio iniciales.
"La práctica clínica actual está peligrosamente desinformada"
Las transfusiones de glóbulos rojos pueden salvar vidas. "Pero no en toda la gama de los umbrales de hemoglobina que actualmente se utilizan para indicar una transfusión", señaló un editorial reciente [11] en el JAMA.Las transfusiones de glóbulos rojos pueden costar vidas también, y es posible, y quizá probable, que lo hagan en algunos casos dentro de los umbrales de hemoglobina y clínicos actualmente en uso. El trauma y las transfusiones son demasiado comunes y demasiado costosos como para que toleremos esta incertidumbre.
Aunque Perel y sus colegas describen su artículo como "informativo para la práctica clínica actual", su valor radica en que nos dice que la práctica clínica actual está peligrosamente desinformada. Lo hace de una manera tal que sugiere persuasivamente que los ensayos futuros acerca de la transfusión en el trauma deben tener en cuenta la gravedad de la presentación de un paciente.
Nuestra base de pruebas para transfusiones en trauma es aún pobre. Con tantos pacientes que mueren cada año, y con las muertes por lesiones que aumentará en importancia a medida que los accidentes de tránsito y las lesiones violentas representan una mayor parte de la carga mundial de la enfermedad [12], tenemos una razón de peso para mejorar y racionalizar nuestras estrategias de transfusión de sangre.