Compresión medular metastásica
Revisión de las causas y presentaciones de la compresión medular metastásica.Autor: Rasha Al-Qurainy , Emily Collis. Metastatic spinal cord compression: diagnosis and management. BMJ 2016;353:i2539
Cinco a 10 de cada 200 pacientes con cáncer terminal sufrirán una compresión medular metastásica (CMM) durante el transcurso de sus 2 últimos años de vida. Es una emergencia oncológica. La CMM está ocasionada por la compresión del saco dural y su contenido (médula espinal o cola de caballo) por una masa extradural o intradural que provoca daños neurológicos irreversibles, como la paraplejia o la tetraplejía, dependiendo del nivel de la lesión. Las más comunes son las masas extradurales.
El colapso medular provocado por la compresión está originado en la diseminación hematógena del cáncer, con la producción de metástasis óseas en la columna vertebral, ocasionando más del 85% de las CMM. Sin embargo, otros dos mecanismos reconocidos son la extensión local del tumor en la médula espinal y la deposición de las células tumorales de un tumor distante directamente dentro de la médula espinal.
Es muy importante el diagnóstico y tratamiento precoz para prevenir el daño neurológico permanente. También es esencial el reconocimiento precoz por los médicos no especializados y la implementación de circuitos de derivación y tratamiento rápidos.
¿Quién sufre una CMM?
"Cualquier tipo de cáncer sistémico puede ocasionar metástasis en la columna vertebral"
Las metástasis vertebrales ocurren en el 3-5% de los pacientes con cáncer, de modo que los pacientes con CMM pueden sufrir dolor y colapso vertebral. La mayoría de las series de adultos destacan que los cánceres de próstata, mama y pulmón representan el 15-20% de cada caso. Sin embargo, prácticamente cualquier tipo de cáncer sistémico puede ocasionar metástasis en la columna vertebral. Una evaluación reciente de las guías de práctica actuales usadas en los hospitales del Reino Unido mostró que el 30% de las derivaciones por CMM comprendían grupos de los diferentes cánceres que más comúnmente se asocian con esta complicación.
En la práctica, no se sabe cuál es la verdadera incidencia de la CMM, ya que la mayoría de los países no tiene una forma sistemática de registrarla. Sin embargo, las evidencias de una auditoría escocesa llevada a cabo hacia finales de la década de 1990, y de un estudio poblacional canadiense indican que la incidencia puede alcanzar 80 casos por millón de personas por año. La guía NICE del Reino Unido informa casi 4.0000 casos por año en Inglaterra y Gales. Debido a que la supervivencia del cáncer aumenta se puede observar un aumento proporcional de la incidencia de CMM, ya que está relacionada con la duración de la enfermedad.
| Lo que necesita saber • La compresión metastásica de la médula espinal es una emergencia oncológica y puede ser la primera presentación de un cáncer. • El estudio de elección es la resonancia magnética de toda la columna vertebral. • Ofrecer corticosteroides y analgésicos y considerar la estabilidad de la columna mientras dura la evaluación del paciente. • Derivación oportuna para neurocirugía o radioterapia, o ambas, lo que proporciona mejores resultados a largo plazo, pero para algunos pacientes la opción terapéutica son los cuidados paliativos |
¿Cómo se presenta?
"El síntoma más común es el dolor de espalda, que ocurre en el 95% de los pacientes"
La CMM puede ser el síntoma inicial del cáncer. Un estudio prospectivo de auditorías de EE. UU. informó que en el 23% de los pacientes con CMM se desconoce la presencia de un cáncer. Un estudio de cohorte retrospectivo más reciente realizado en el Reino Unido informó que el 21% (27/127) de los pacientes con CMM que fue derivado a un centro oncológico de Londres durante 1 año no tenía diagnóstico previo de cáncer. La CMM puede ser particularmente difícil de diagnosticar en las personas con mal estado funcional, edad avanzada o comorbilidades.
Dolor
El síntoma más común es el dolor de espalda, que ocurre en el 95% de los pacientes hasta 2 meses antes de la presentación de los signos relacionados con la aparición de la CMM. El dolor puede estar localizado (en y alrededor de la columna vertebral) o ser radicular (dolor provocado por la afectación de la raíz nerviosa de uno o ambos lados del cuerpo). En una auditoría escocesa de 319 pacientes con CMM, el 37% tenía dolor radicular, el 15% dolor localizado en la columna y el 47% ambos. Los pacientes pueden relatar dolor torácico inferior y dolor radicular lumbar superior como también dolor abdominal.
Con frecuencia, el dolor aumenta en intensidad a lo largo del tiempo y puede ser peor al hacer fuerza o toser o al acostarse, debido a la distensión del plexo epidural. A menudo es difícil distinguir a las personas en riesgo de CMM de las personas con dolor de espalda simple. La guía NICE del Reino Unido recomienda tener un elevado índice de sospecha en aquellas personas con un diagnóstico de cáncer conocido o con dolor incesante y grave, especialmente si se localiza en la columna vertebral superior o media, o el dolor es agravado por el aumento de la presión intraabdominal. También puede ser difícil distinguir el dolor provocado por las metástasis medulares del dolor por compresión de la médula. La guía NICE del Reino Unido proporciona la lista de verificación que figura a continuación.
Recomendaciones del NICE para el diagnóstico y tratamiento de los pacientes con riesgo de CMM o con metástasis vertebrarles
• Póngase en contacto urgente (24 horas) con el equipo correspondiente (de ser posible, a través de un coordinador de CMM designado) para discutir la atención de los pacientes con cáncer y dolor que presenten cualquiera de las siguientes características sugerentes de metástasis vertebrales:
- Dolor en la columna vertebral media (tórácica) o superior (cervical).
- Dolor vertebral inferior (lumbar) progresivo.
- Dolor intenso e incesante en la columna baja.
- Dolor vertebral agravado por el esfuerzo (por ej., defecación) o al toser o estornudar.
- Dolor vertebral localizado.
- Dolor espinal nocturno que impide dormir.
- Dolor en la columna vertebral media (tórácica) o superior (cervical).
- Dolor vertebral inferior (lumbar) progresivo.
- Dolor intenso e incesante en la columna baja.
- Dolor vertebral agravado por el esfuerzo (por ej., defecación) o al toser o estornudar.
- Dolor vertebral localizado.
- Dolor espinal nocturno que impide dormir.
• Contactarse inmediatamente con el coordinador de CMM (o equivalente) para discutir la atención de los pacientes con cáncer y síntomas sugestivos de metástasis vertebrales, que tienen cualquiera de los siguientes signos o síntomas neurológicos sospechosos de CMM y considerar el cuadro como una emergencia oncológica:
- Síntomas neurológicos (incluyendo dolor radicular, cualquier debilidad en las extremidades, dificultad para caminar, pérdida de la sensibilidad y disfunción vesical o intestinal.
- Signos neurológicos de compresión medular o de la cola de caballo.
• Realizar revisiones clínicas frecuentes (diarias, dependiendo del cuadro) de los pacientes con cáncer que desarrollan dolor en la columna baja, de origen clínicamente inespecífico (es decir, no es progresivo ni grave o no se agrava por el esfuerzo, y no tiene síntomas neurológicos acompañantes).
En particular busque:
- Desarrollo de progresivo de dolor u otros síntomas sugestivos de metástasis vertebrales (contactarse con el coordinador de CMM dentro de las 24 horas).
- Desarrollo de síntomas neurológicos o signos sugestivos de CMM (contactarse de inmediato con el coordinador de CMM)
- Síntomas neurológicos (incluyendo dolor radicular, cualquier debilidad en las extremidades, dificultad para caminar, pérdida de la sensibilidad y disfunción vesical o intestinal.
- Signos neurológicos de compresión medular o de la cola de caballo.
• Realizar revisiones clínicas frecuentes (diarias, dependiendo del cuadro) de los pacientes con cáncer que desarrollan dolor en la columna baja, de origen clínicamente inespecífico (es decir, no es progresivo ni grave o no se agrava por el esfuerzo, y no tiene síntomas neurológicos acompañantes).
En particular busque:
- Desarrollo de progresivo de dolor u otros síntomas sugestivos de metástasis vertebrales (contactarse con el coordinador de CMM dentro de las 24 horas).
- Desarrollo de síntomas neurológicos o signos sugestivos de CMM (contactarse de inmediato con el coordinador de CMM)
• Realizar revisiones clínicas frecuentes de los pacientes sin un diagnóstico previo de cáncer que desarrollan dolor vertebral sospechoso (con las características indicadas más arriba) con o sin síntomas neurológicos.
Tratar o derivar a los pacientes con síntomas leves y estables por la vía de atención vertebral normal no específica, o referir al oncólogo para tratamiento, si es necesario. En particular, busque:
- Desarrollo de dolor progresivo u otros síntomas sugestivos de metástasis vertebrales (contactarse con el coordinador de la CMM dentro de las 24 horas).
- Desarrollo de síntomas neurológicos o signos sugestivos de CMM).
Tratar o derivar a los pacientes con síntomas leves y estables por la vía de atención vertebral normal no específica, o referir al oncólogo para tratamiento, si es necesario. En particular, busque:
- Desarrollo de dolor progresivo u otros síntomas sugestivos de metástasis vertebrales (contactarse con el coordinador de la CMM dentro de las 24 horas).
- Desarrollo de síntomas neurológicos o signos sugestivos de CMM).
Esta lista permite distinguir entre ambos tipos de dolor. Para aquellos que solo presentan dolor (en los que se sospecha metástasis vertebral) se recomienda la resonancia nuclear magnética (RMN) de toda la columna vertebral dentro de los 7 días. Para los pacientes con dolor y signos neurológicos que despiertan sospecha de CMM, se recomienda la RNM de toda la columna dentro de las 24 horas.
Déficit motor
El segundo síntoma más común es la debilidad de las extremidades, que afecta al 60-85% de los pacientes en el momento del diagnóstico de CMM. Los pacientes pueden quejarse de marcha inestable o de un rápido inicio de la dificultad para estar parado, caminar o trasladarse de la cama a la silla, o sus síntomas han progresado a lo largo de los días o de unas pocas semanas. Los pacientes frágiles con enfermedad avanzada no pueden hacer notar su debilidad, pero los cuidadores pueden observar el deterioro repentino de la capacidad funcional.
La mayoría de las guías publicadas se centran en la importancia de reducir al mínimo el déficit antes de iniciar el tratamiento, en un intento de prevenir la paraplejía. El predictor más fuerte del resultado neurológico del tratamiento es el estado neurológico al iniciar el tratamiento. Un importante estudio retrospectivo de cohorte, bien diseñado, halló una asociación entre el desarrollo más lento del déficit motor previo al inicio de la radioterapia y un mejor resultado funcional después del tratamiento.
Déficits sensoriales
Los síntomas sensoriales son menos comunes y pueden presentarse antes de que los signos sensoriales se hagan evidentes. Los pacientes pueden quejarse de parestesias, disminución de la sensibilidad y entumecimiento de los dedos del pie y de las manos, lo cual puede extenderse 1-5 dermatomas por debajo del verdadero nivel de la compresión medular.
La pérdida de la sensibilidad radicular y de los reflejos tendinosos en el examen clínico permite establecer el nivel anatómico de la compresión más exactitud que los síntomas subjetivos. La presentación de los síntomas sensitivos y motores desde el inicio debe despertar un elevado grado de sospecha de CMM.
Disfunción autonómica
A menudo, esta disfunción es una consecuencia tardía de la CMM y puede presentarse como disfunción de la vejiga y del intestino (retención urinaria, incontinencia urinaria, incontinencia fecal, constipación). Se recomienda hacer un interrogatorio directo para excluir esta disfunción (por ej., "¿Es capaz de evacuar el intestino y orinar normalmente?" "¿Ha tenido algún episodio de pérdida involuntaria de materia fecal u orina sin previo aviso? ").
Los pacientes con enfermedad avanzada pueden tener estreñimiento multifactorial (por ej., por inmovilidad o analgesia), lo que también pueden afectar adversamente la función de la vejiga. En una auditoría prospectiva, el síntoma intestinal más frecuente fue el estreñimiento y ocurrió en el 67% de los pacientes con CMM.
Síndrome de la cola de caballo
El sitio de la lesión está por debajo de la primera vértebra lumbar. Los pacientes con síndrome de la cola de caballo se presentan de diferentes maneras. A menudo, relatan la disminución de la conciencia al comenzar a orinar o defecar, sin déficit motor y, a veces, en ausencia de dolor. Los principales signos clínicos son la disminución de la sensibilidad en las nalgas, la cara posterosuperior de los muslos y la región perineal, con una distribución en silla de montar. En el examen físico, la mayoría de los pacientes muestra una disminución del tono del esfínter anal. La retención urinaria con incontinencia por rebosamiento es un predictor importante, con una sensibilidad del 90% y una especificidad del 95%.
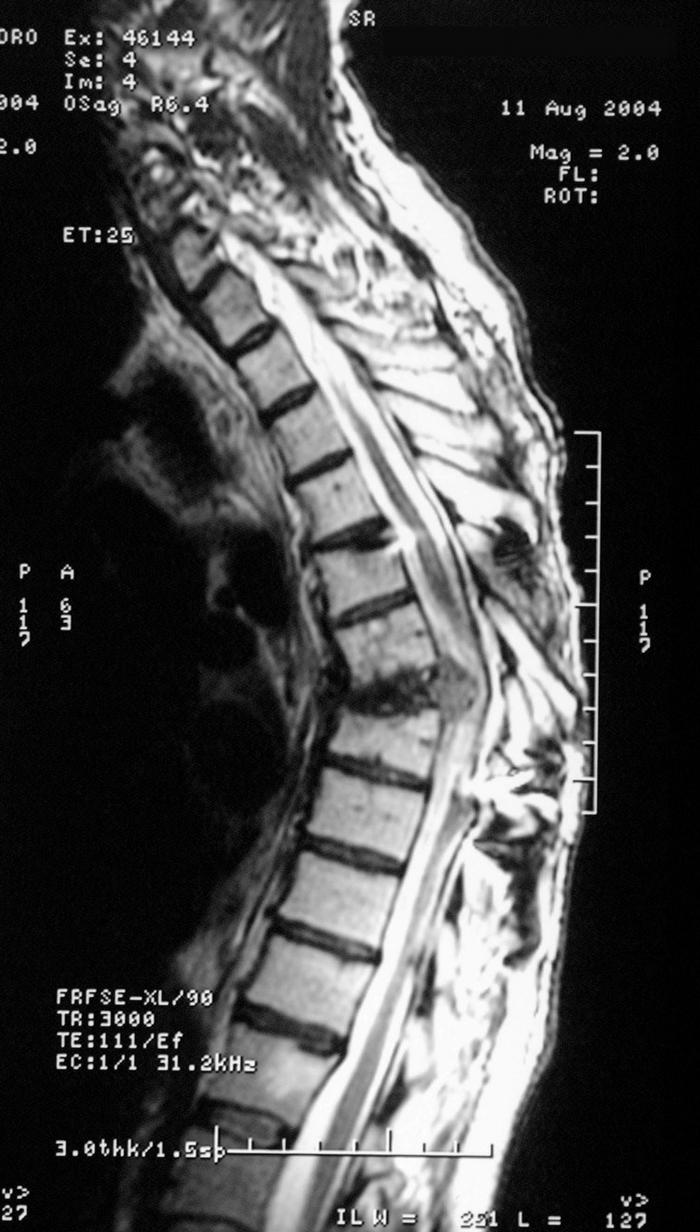 ¿Cómo se confirma el diagnóstico?
¿Cómo se confirma el diagnóstico?
El método de imagen de elección es la RNM de toda la columna vertebral, ya que tiene una sensibilidad del 93% y una especificidad del 97%. En consecuencia, se dejará de hacer el diagnóstico solo en unos pocos pacientes (7%) mientras que un número más pequeño (3%) tendrá un resultado positivo falso. En el Reino Unido, la guía NICE recomienda hacer la RNM dentro de las 24 horas de la sospecha clínica. Muchos centros oncológicos de ese país cuentan con un canal de atención dedicado a los pacientes remitidos desde la comunidad, lo que permite hacer estudios por imagen, tomar decisiones por parte de un equipo multidisciplinario y hacer el tratamiento de manera oportuna, supervisado por un coordinador para las CMM especialmente designado (se haya establecido o no el diagnóstico de cáncer).
La tomografía computarizada (TC) suele ser utilizada para ayudar a planificar el tratamiento quirúrgico o radioterápico, pero no se recomienda para el diagnóstico definitivo de la CMM. En la actualidad, raramente se utiliza la mielografía por TC, salvo para aquellos pacientes con contraindicaciones para la RNM. El centellograma óseo y la radiografía simple no son útiles para el diagnóstico.
¿Cuándo se debe evitar investigar o tratar?
En algunas situaciones en las que se sospecha la CMM podría ser más adecuado no investigar o tratar, como sucede cuando hay poca o nula perspectiva de un resultado favorable, y después de haber discutido ampliamente con el paciente sobre los beneficios y las cargas de la enfermedad y el tratamiento. Tales situaciones incluyen la parálisis bien establecida de más de una semana de duración, el mal estado general de base y una expectativa de vida útil dada por la enfermedad subyacente de solo unos días o semanas. En estos casos, deben considerarse los cuidados paliativos, lo que implica la indicación empírica de corticosteroides (8 mg de dexametasona oral o subcutánea, 2 veces/día) como tratamiento de elección.
¿Qué se debe hacer mientras se espera del diagnóstico?
El consejo actual es administrar esteroides y analgésicos, e indicar el reposo para proteger la alineación de la columna vulnerable de un daño posterior mayor y, la inmovilización adecuada.
¿Cuál es el papel de los esteroides?
La evidencia de ensayos aleatorizados y controlados indica que los corticosteroides proporcionan un tratamiento coadyuvante beneficioso para los pacientes con mielopatía epidural compresiva. Un estudio aleatorizado detectó tasas de deambulación más elevadas en los pacientes con CMM que recibieron dexametasona antes de la radioterapia, en comparación con aquellos que no lo hicieron (81% vs. 63% a los 3 meses).
Las guías del Reino Unido recomiendan que, salvo contraindicación, todos los pacientes con CMM deben recibir una dosis de carga inmediata de 16 mg de dexametasona (vía iv. u oral) seguida de un ciclo corto de 16 mg de dexametasona/día (en dosis divididas, por ej. 8 mg, 2 veces/día, por vía oral). Si la causa probable de la CMM es el linfoma, los esteroides están contraindicados ya que su efecto oncolítico puede alterar el diagnóstico tisular.
Las recomendaciones canadienses aconsejan administrar 16 mg de dexametasona diarios, tan pronto como se sospecha la CMM y desaconsejan el uso de dosis más elevadas de corticosteroides. Esta recomendación está de acuerdo con los hallazgos de un estudio prospectivo noruego que informó una elevada incidencia de efectos secundarios graves y ningún beneficio para la deambulación con el uso de dosis más elevadas (96 mg) de dexametasona.
La evidencia anecdótica sugiere que los pacientes que responden neurológicamente a la iniciación de la terapia con esteroides tienden a responder mejor a la radioterapia.
Suspensión de los esteroides
Los corticosteroides pueden proporcionar un beneficio analgésico y una mejoría inicial de la función neurológica. Sin embargo, los beneficios a largo plazo son limitados, sin que se haya encontrado evidencia de la mejoría de la supervivencia y con efectos secundarios indeseables que pueden ser debilitantes y algunas veces fatales.
Después de la cirugía o la radioterapia, las guías del Reino Unido recomiendan la disminución gradual de las dosis de esteroides y su suspensión completa al cabo de 4-6 semanas o, llegar a la dosis de mantenimiento más baja que permita la estabilidad de los síntomas. En los pacientes que no fueron sometidos a cirugía o radioterapia, la dexametasona debe reducirse hasta finalmente suspenderla. En este caso, un estudio noruego aconseja reducir la dosis con mayor rapidez a partir de los 16 mg hasta llegar a 0 mg en 14 días.
Una auditoría prospectiva a gran escala del Reino Unido, realizada en hospitales, mostró que la dosis de esteroides no fue revisada periódicamente y que los pacientes a menudo se mantuvieron bajo tratamiento esteroide de manera inapropiada, lo que dio como resultado que el 40% experimentara efectos secundarios, comúnmente miopatía periférica más proximal y edema.
¿Qué analgésicos deben prescribirse?
En general, el dolor asociado a la CMM es tanto óseo como neuropático. El mecanismo del dolor óseo se produce parcialmente a través de mediadores inflamatorios y por lo tanto responde bien al tratamiento con esteroides. Para guiar la analgesia se debe utilizar la escala de dolor de la OMS, con el uso adecuado de analgésicos adyuvantes neuropáticos. En caso de necesidad, se debe buscar el asesoramiento de especialistas en dolor o del equipo de cuidados paliativos y considerar la prescripción tanto de la analgesia regular como de la analgesia "según necesidad".
Alineación
Independientemente de la distribución, para los pacientes con dolor severo provocado por el movimiento, lo que sugiere la inestabilidad espinal, o con cualquier síntoma o signo neurológico sugestivos de CMM, lo ideal es alinear la columna en forma neutra (incluyendo la maniobra de rotación del paciente con el uso de un chata deslizante para ir al baño) hasta que esté asegurada la estabilidad ósea y neurológica (idealmente después de la RNM y la revisión neuroquirúrgica), pudiendo comenzar la recuperación cautelosa de la movilidad con la participación de un fisioterapeuta.
Tratamiento
El tratamiento definitivo puede incluir cualquier combinación de radioterapia, cirugía y quimioterapia. Si la terapia es adecuada y el paciente lo acepta, se debe iniciar antes de que se produzca otro deterioro neurológico y, preferentemente, dentro de las 24 horas del diagnóstico confirmado de CMM.
Como orientación para los planes terapéuticos es importante que los pacientes tengan un diagnóstico histológico o citológico de neoplasia maligna. Si este diagnóstico no estuviese confirmado con anterioridad, está indicada la biopsia con aguja o la biopsia a cielo abierto, tan pronto como sea posible, antes de la radioterapia o la cirugía.
Al decidir junto con el paciente sobre el tratamiento definitivo, hay que tener en cuenta su estado general, el grado de enfermedad metastásica, la estabilidad de la columna, la radiosensibilidad del tumor subyacente y, el grado de compresión de la médula espinal.
Radioterapia
Históricamente, la radioterapia ha sido considerada un tratamiento de primera línea ya que se ha demostrado que es tan eficaz como la laminectomía descompresiva, con una incidencia más baja de complicaciones. Los resultados también mejoran (incluyendo la reducción de las tasas de recurrencia local) después de la cirugía y en los pacientes que no son candidatos a la cirugía. Los 3 objetivos terapéuticos de la radioterapia son:
• Prevennir el deterioro neurológico
• Mejorar la función neurológica
• Aliviar el dolor.
• Mejorar la función neurológica
• Aliviar el dolor.
Para los pacientes con buen pronóstico (ambulantes o con inmovilidad <24 horas), está indicado un tratamiento urgente dentro de las 24 horas del diagnóstico. En todo el mundo se utilizan muchos regímenes de radioterapia, con el consenso actual de utilizar 20 Gy en 5 fracciones diarias o 30 Gy en 10 fracciones diarias. Este tratamiento podrá reducir el riesgo de recurrencia en el campo.
Los pacientes con mal pronóstico son los que tienen menos de 6 meses la esperanza de vida, mal estado funcional y una paraplejia de más de 24 horas de duración. En estos pacientes, la mediana de la supervivencia es de 1-2 meses, con pocas probabilidades de recuperación de los trastornos neurológicos. La radioterapia solo se indica para aliviar el dolor, pero en casos raros, algunos pacientes pueden mostrar la recuperación neurológica. Es adecuada una dosis única de 8 Gy.
Un ensayo aleatorizado informó un resultado funcional similar con la aplicación de los 3 esquemas de radioterapia diferentes, pero la dosis única de radiación se asoció con mayor recurrencia en el campo.
Cirugía
Los objetivos de la cirugía son lograr una descompresión circunferencial de la médula espinal y, reconstruir y estabilizar inmediatamente la columna vertebral. Un número creciente de evidencia indica que la cirugía es superior a la radioterapia para conservar o recuperar la función neurológica y aliviar el dolor. Un ensayo aleatorizado y controlado de EEE. UU. informó que 42/50 (84%) pacientes asignados al azar a la neurocirugía más radioterapia posoperatoria lograron el objetivo principal que es mejorar la capacidad para caminar al finalizar el tratamiento, en comparación con 29/51 (57%) de los pacientes asignados al azar a la radioterapia sola.
La elección de la cirugía comparada con otros tratamientos puede ser difícil de determinar. Las discusiones con los pacientes deben tener en cuenta su estado general, el pronóstico y las preferencias. Cada vez más los cirujanos basan sus decisiones en los puntajes objetivos basados en el pronóstico, como los puntajes Tomita y Tokuhashi modificado. Los pacientes con inestabilidad de la columna, buena esperanza de vida o con tumores resistentes a la radioterapia son propensos a tener resultados neurológicos mucho mejores si antes de la radiación se procede a la resección del tumor y la estabilización de la médula.
El Spinal Instability Neoplastic Score (SINS) (Puntaje de Estabilidad Nepplásica Espinal) es una herramienta validada para determinar la inestabilidad clínica (definida como "pérdida de la integridad de la médula como resultado de un proceso neoplásico asociado al dolor relacionado con el movimiento, la deformidad sintomática o progresiva y/o el compromiso neuronal bajo cargas fisiológicas").
Una revisión sistemática canadiense no halló ninguna evidencia directa que apoye el tipo de cirugía a realizar ni si debe intentarse una cirugía de salvataje cuando el paciente muestra progresión de la enfermedad durante la radioterapia o poco después de ella. Los revisores aconsejan tener en cuenta el tratamiento ambulatorio previo, las comorbilidades, los factores técnicos quirúrgicos, la presencia de compresión ósea y la inestabilidad la médula, las posibles complicaciones quirúrgicas o de la radioterapia y, las preferencias del paciente.
El momento de la intervención quirúrgica también ha sido objeto de debate. Un estudio reciente chino, retrospectivo, pequeño, indica que la cirugía puede beneficiar a los pacientes, incluso si no caminan, siempre que se realice dentro de las 48 horas de realizado el diagnóstico de CMM.
Quimioterapia
La quimioterapia puede tener un papel en el manejo de las neoplasias quimiosensibles como el linfoma, los tumores de células plasmáticas, los tumores de células germinales y el carcinoma de pulmón de células pequeñas.
Rehabilitación
Rehabilitación
La planificación del alta y la atención continua, incluida la rehabilitación, comienzan en la admisión y lo ideal es que esté coordinada por un individuo designado dentro del equipo clínico. El éxito depende del paciente y sus cuidadores, los equipos de oncología y rehabilitación y el apoyo de la comunidad, incluida la atención primaria y los cuidados paliativos, según sea necesario. La meta es centrarse en los objetivos para la atención del paciente, con el fin de maximizar la función física en el contexto de la calidad de vida en general. La rehabilitación debe ser proporcionada en el lugar preferido para la atención del paciente. Por lo general, se inicia en el establecimiento de agudos y luego se continúa en la comunidad, en el hospicio o, en la unidad de rehabilitación hospitalaria especializada.
Calidad de vida
Poco se sabe sobre el impacto psicológico de la CMM. Una revisión reciente de la literatura mediante el análisis temático concluyó que más del 50% de los pacientes con CMM informa una buena calidad de vida y niveles bajos de angustia, y solo una minoría relata dificultades graves. Se requiere mayor conciencia y más investigación del impacto psicológico para determinar los grupos de riesgo y las estrategias más efectivas para su apoyo.
Preguntas para el futuro
• ¿La radioterapia estereotáctica mejora la movilidad de los pacientes con metástasis medulares de tumores radio resistentes o de los pacientes que han recibido radioterapia estándar previa?
• ¿La intervención quirúrgica precoz reduce la incidencia de CMM en los pacientes con metástasis vertebrales?
• ¿La vertebroplastia o la cifoplastia reducen la incidencia de CMM en los pacientes con metástasis vertebrales?
• ¿Cuál es el régimen de radioterapia clínicamente más eficaz y rentable para el tratamiento de los pacientes con CMM establecida?
• ¿La intervención quirúrgica precoz reduce la incidencia de CMM en los pacientes con metástasis vertebrales?
• ¿La vertebroplastia o la cifoplastia reducen la incidencia de CMM en los pacientes con metástasis vertebrales?
• ¿Cuál es el régimen de radioterapia clínicamente más eficaz y rentable para el tratamiento de los pacientes con CMM establecida?
Traducción y resumen objetivo: Dra. Marta Papponetti





